[分迪观点]:通过肽库筛选和药物化学的结合,波恩大学的研究人员成功发现了一类新的具有细胞渗透性和Gαi/s 选择性的肽基调节剂,能够可逆地调节Gα 蛋白活性,为 Gαi/s 直接调节剂的开发证明了可行性。
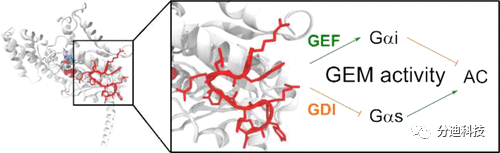
迄今为止,只有 FR900359 (FR) 和 YM-254890 (YM)等少数特定的 G 蛋白调节剂是已知的,而且它们均为靶向 Gαq 的天然环状肽。受此启发,研究人员筛选了一株一物化学组合多肽库 (OBOC) ,从中发现了一种相对有效的 Gαi1·GDP 调节剂 GPM-1。
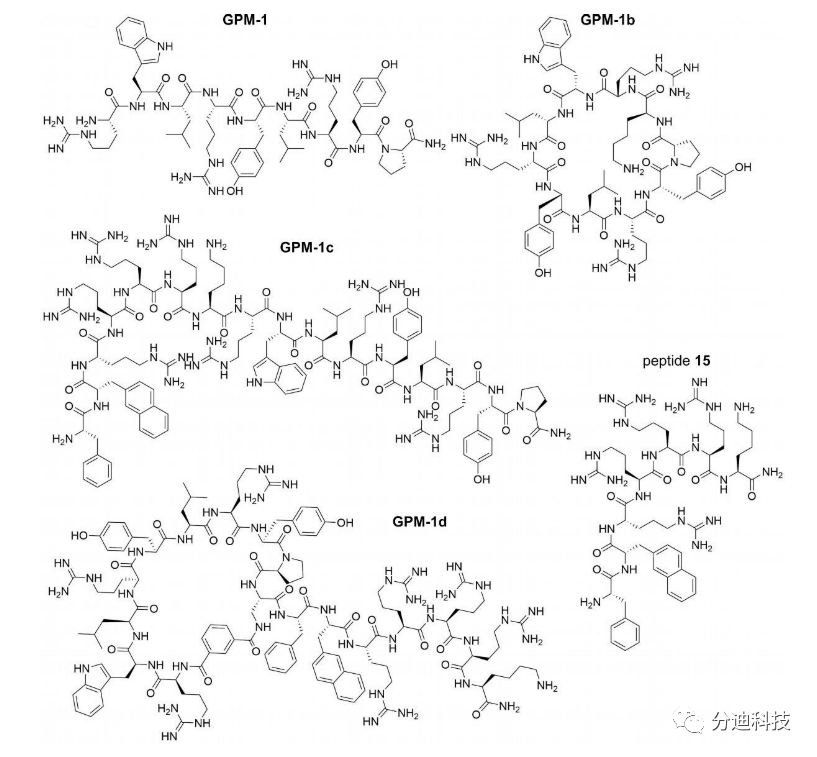
随后对 GPM-1 进行优化提高其结合亲和力和蛋白水解稳定性,并与细胞穿透肽 (CPP) 结合提高其细胞渗透性。研究结果表明,GPM-1 的变体GPM 1c 和 GPM-1d 可以通过类似鸟嘌呤-核苷酸交换调节剂(GEM) 的方式调节细胞培养中的 Gαi/s 活性,即作为 Gαi 的鸟嘌呤核苷酸交换因子 (GEF) 和 Gαs 的鸟嘌呤核苷酸解离抑制剂 (GDI),具有双功能活性。
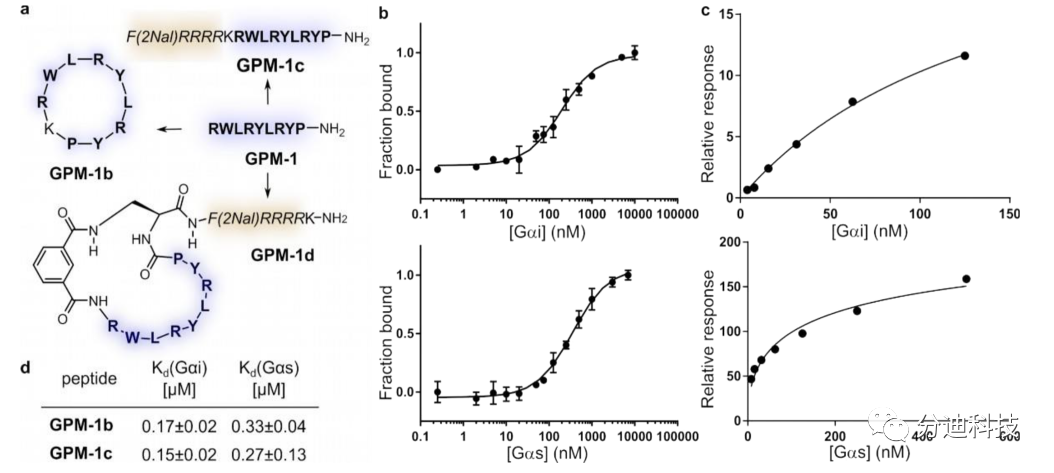
为了深入了解多肽的生物活性结构基础,研究人员对 Gαi/s 与实验上被认为具有活性的肽调节剂(GPM-1c、GPM-1d)的相互作用进行了一系列计算分析。首先,通过 YASARA 生成Gαi1以及GPM-1 和GPM-1b-d等肽的3D结构,后通过 SeeSAR 中的 DoGSiteScorer 算法预测肽可能性的结合位点,并通过 YASARA 中的VINA算法进行对接。
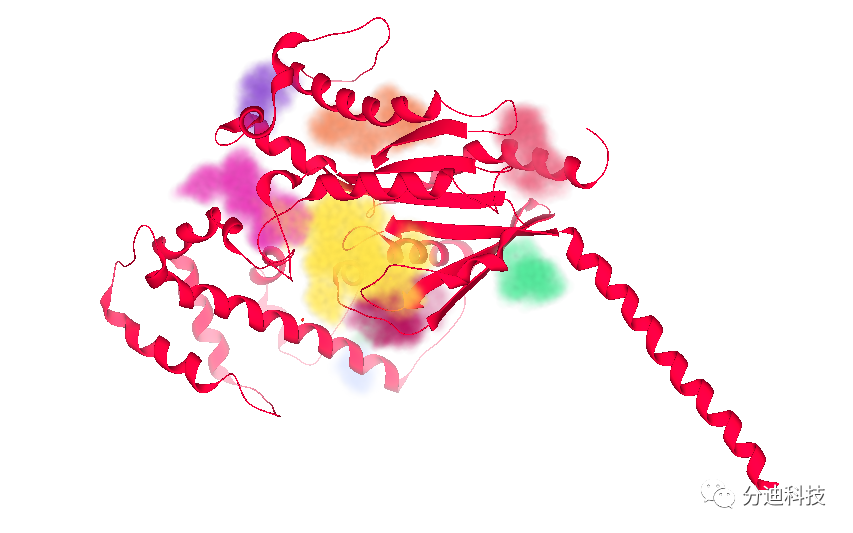
DoGSiteScorer 预测的结合口袋
随后对 GPM-1c 与 Gαi/s 结合后 GDP 的结合亲和力变化进行视觉评估,其中原子对结合亲和力的贡献由 SeeSAR 中的 HYDE 评分函数计算。绿色球体表示对结合亲和力有积极的贡献,红色球体表示对结合亲和力有不利的贡献,球体的大小和影响成正比。
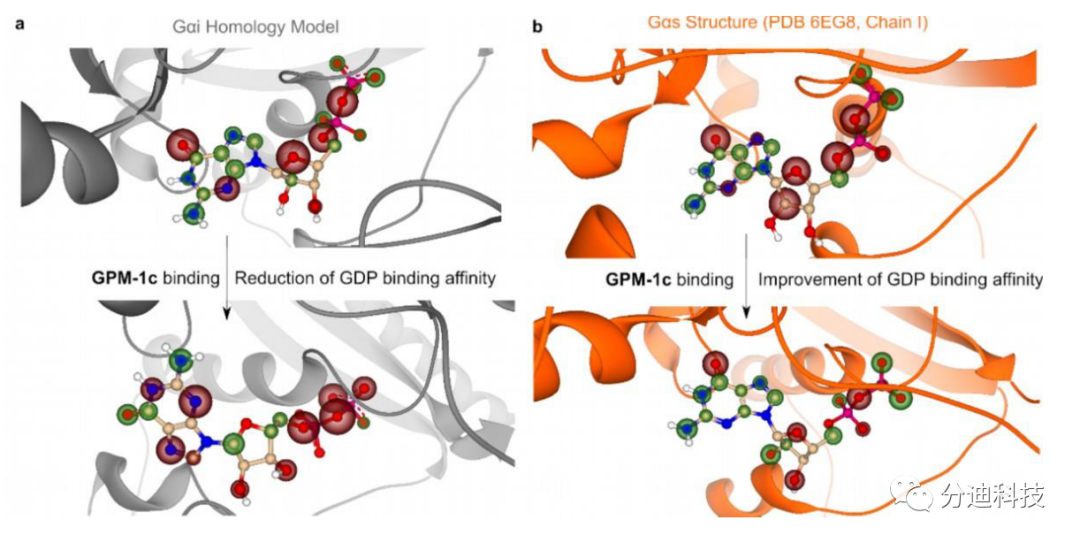
HYDE 评估结合亲和力
在 a 和 b 中,顶部结构表示初始结构,下部表示MD 50ns 后的结构。从图中可以看出,GPM-1c 和 Gαi 结合后,红色的球体整体增加(左侧灰色),表明 GDP 和 Gαi 之间不利的相互作用增加,即肽的结合可能促进 Gαi 释放 GDP,具有类似 GEF 的作用。GPM-1c 和 Gαs 结合前后的情况则相反,红色的球体整体减少(右侧橘红色),表明 GDP 和 Gαs 之间不利的相互作用降低,即 GPM-1c 改善了 GDP 与 Gαs 的结合,具有类似 GDI 的作用。
参考资料
Targeting Gαi/s Proteins with Peptidyl Nucleotide Exchange Modulators
https://pubs.acs.org/doi/10.1021/acschembio.1c00929

